En injektionsbehandling som prövats på möss gör immunceller till ett vapen mot cancer
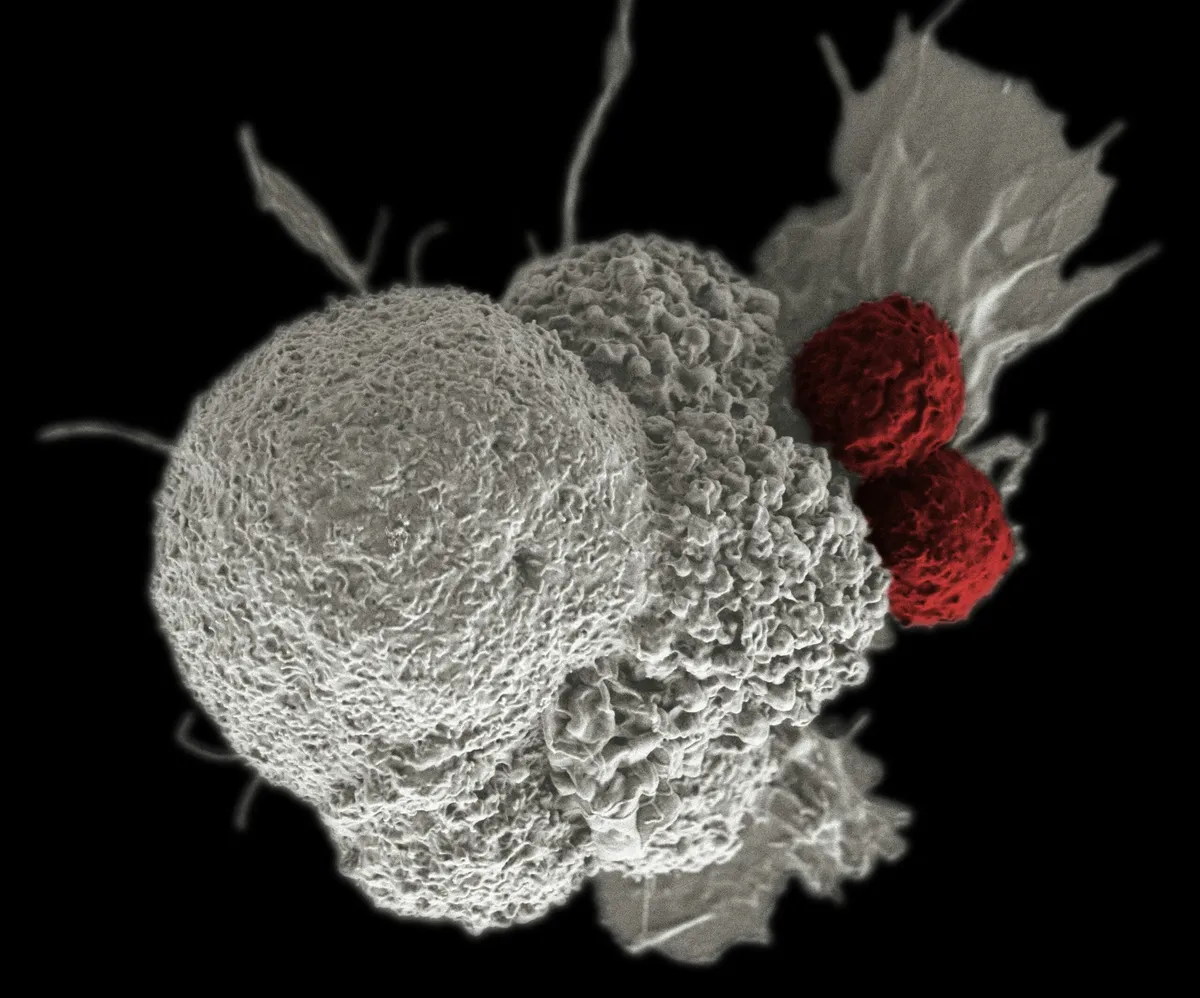
En ny genterapiteknik skulle kunna ändra spelreglerna för cancerbehandling genom att omprogrammera immunceller direkt i kroppen så att de attackerar tumörutplåning. Metoden är särskilt intressant för CAR‑T‑terapier som produceras in vivo (där cellerna bildas i kroppen), eftersom den kan göra behandlingarna mer tillgängliga och billigare för patienter världen över.
Vad som begränsar dagens CAR‑T‑behandlingar
Dagens CAR‑T‑terapier har spelat en viktig roll mot blodcancer de senaste åren, och metoden bygger på att patientens T‑lymfocyter först tas ut, modifieras i labbet för att känna igen och attackera T-cellsengagerare. Processen tar ofta flera veckor och är mycket kostsam, i USA ligger kostnaden på mellan 4 600 000 kr och 5 750 000 kr per patient. Dessutom krävs specialiserade anläggningar, vilket innebär att bara stora cancercentrum för närvarande kan erbjuda behandlingarna.
En ny väg i cancerbehandling
Professor Justin Eyquem och hans team vid University of California, San Francisco (UCSF) har tagit fram en ny metod som publicerades i tidskriften Nature den 18 mars. De injicerar två partiklar direkt i blodet: den ena transporterar CRISPR-Cas9-redigeringsmaskineriet riktat mot cirkulerande T‑lymfocyter, den andra levererar DNA för den anticancer‑CAR‑receptorn. På så sätt minskar behovet av att ta ut och manipulera immunceller utanför kroppen, vilket förenklar och snabbar upp hela processen.
Resultaten i djurförsök
Djurstudierna visar mycket starka resultat. En enda injektion med tvåpartikelsystemet rensade bort all detekterbar leukemi i nästan alla behandlade möss inom två veckor. Metoden fungerade även mot multipelt myelom och mot solida tumörer som sarkom, områden där traditionella CAR‑T‑terapier ofta faller kort. I vissa organ utgjorde de in vivo‑framställda CAR‑T‑cellerna upp till 40 % av immuncellerna som fanns där, vilket tyder på att mössens egna kroppar blev fungerande “produktionsanläggningar” för behandlingen.
Bättre säkerhet och effektivitet
Genom att CRISPR‑Cas9 integrerar CAR‑DNA på bestämda platser i genomet får metoden en tydlig säkerhetsfördel jämfört med tekniker som ofta orsakar slumpmässiga insättningar av genetiskt material. Det minskar risken för sekundära cancerformer och gör tekniken både säkrare och mer träffsäker.
Justin Eyquem kommenterade att cellerna som modifieras i kroppen “verkar till och med bättre än de vi tillverkar i laboratoriet”. Den observationen tyder på att in vivo‑modifierade celler kan prestera bättre än de som skapas i labbmiljö.
Framtiden och utmaningarna
Om metoden visar sig fungera hos människor kan både produktionstiden och kostnaderna minska kraftigt, vilket skulle göra det möjligt för också närsjukhus att erbjuda dessa livsviktiga behandlingar, inte bara stora cancercenter, och främja tidiga diagnoser. Trots de lovande prekliniska resultaten krävs dock flera år av rigorösa kliniska prövningar för att säkerställa att metoden är säker och effektiv hos människor.
Vilka som ligger bakom och hur regelverket ser ut
Studien är ett samarbete mellan UCSF, Gladstone Institutes, Duke University och Innovative Genomics Institute, som medgrundats av CRISPR‑pionjären Jennifer Doudna. I nuläget har den amerikanska FDA godkänt sju CAR‑T‑terapier för behandling av blodcancer, men ingen av dem är effektiv mot solida tumörer, och sådana tumörer står för en majoritet av cancerfallen globalt.
Denna nya teknik kan utgöra ett potentiellt paradigmskifte inom cancerbehandling, med löftet att bryta barriärer och föra möjligheten till effektiv behandling närmare patienter oavsett var de bor. Förhoppningen är att göra dessa avancerade behandlingar tillgängliga på ett sätt som tidigare var omöjligt.